INTRODUZIONE
ALL'ATOMISTICA

storia della chimica dal VI secolo a.C. al XVII d.C.
Le conoscenze chimiche degli antichi ci sono pervenute attraverso il mondo dei Greci, poiché i nostri contatti con la Cina, la Persia, l'India, la Mesopotamia e l'Egitto sono sempre state inibite dalla scarsa conoscenza dei loro scritti e dalle relazioni soprattutto commerciali o belliche con questi centri di civiltà antica. I filosofi Greci del periodo VI-III secolo a.C. (finché la loro terra non cadde sotto il dominio di Roma) concepirono una serie di teorie che sarebbero rimaste quasi intatte per altri 10-12 secoli. In parte le loro idee passarono attraverso gli Arabi che fino al XII secolo erano tutt'altro che oscurantisti e non esitavano a tradurre dal greco in arabo ciò che per il cristianesimo di allora sarebbe stata e per l'islamismo di oggi sarebbe un'opera del Diavolo. Tramite le opere arabe tradotte alle corti europee di Lisbona, Sevilla, Londra (per citarne solo alcune) la futura CHIMICA del XVII secolo si arricchì anche di alcune idee di antica origine orientale (Cina o India). Sorvoleremo brevemente sui concetti di maggiore impatto sullo sviluppo del sapere della materia, lasciando agli interessati il piacere di scoprire da soli il mondo incredibile degli alchimisti medioevali!
 |
Considerando la percentuale di acqua della superficie terrestre (circa 70%) e il suo contenuto negli esseri viventi (60-70%), come dargli torto? |
 |
Considerando il concetto moderno di energia come un'altra faccia della materia e il fatto che il calore (fuoco) consiste in microonde e in onde infrarosse, come dargli torto? |
 |
|
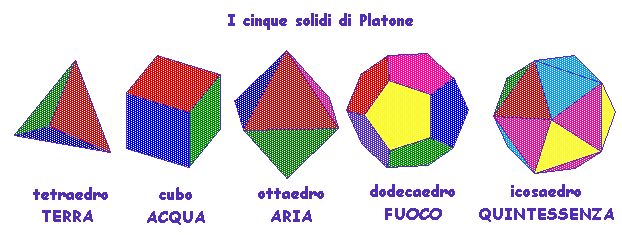
Platone abbinò il concetto dei 4 elementi
+ quintessenza alla scoperta dei solidi fondamentali:
 |
|
L'idea originale dell'indistruttibilità proviene da Anassimandro (611-546 a.C.) che riteneva tutto costituito da una sostanza fondamentale, indefinita e indistruttibile, detta APERION. Democrito aggiunse anche una spiegazione per come gli atomi si legano per formare le cose che osserviamo nel mondo: tramite minuscoli ganci e occhielli!
 |
Pensando al lavoro odierno della fisica atomica, come dargli torto: dopo aver frantumato l'atomo in 3 particelle subatomiche, da queste ultime si ottiene una serie infinita di mesoni, fotoni, leptoni, quark, anti-quark! |
 |
|
Il tipico diagramma aristoteliano dei 4 elementi
e 4 caratteri:
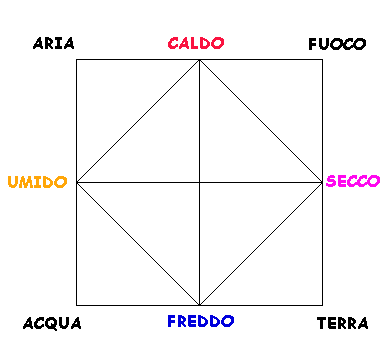
Aristotele, maestro del ragionamento logico
per induzione, respinse le teorie atomistiche, perfezionò il proprio
modello ed accettò il principio della trasmutazione dei metalli.
In effetti questo pensiero, alla base di 1 000 anni di alchimia, è
perfettamente logico se si accetta la teoria dei 4 elementi con l'aggiunta
della quintessenza o pietra filosofale (chiamata anche flogistone o flogisto),
il quinto elemento che fonde gli altri 4. Non mancavano le esperienze concrete!
Il cinabro (nella foto sotto di color arancione-marrone),
ritenuto un metallo per l'aspetto e la durezza, ma in realtà un
minerale composto di mercurio e zolfo, si lascia trasformare in mercurio
puro (gocce argentee nella foto) per reazione al calore e alla presenza
di ossigeno. Lo zolfo finisce nell'ossido (anidride solforosa) che svanisce
nell'aria. Con il medesimo procedimento si può ricavare ferro dal
minerale pirite contenente ferro e zolfo, ma che sembra un metallo. Questo
fu alla base della teoria che riteneva il mercurio il solo metallo puro
e tutti gli altri costituiti da variabili miscugli di mercurio e zolfo.
Allora bastava scoprire il segreto, isolare il quinto elemento, per avere
la ricetta (percentuali di mercurio e zolfo) della trasformazione del piombo
in oro! Così si provò inutilmente per secoli, poiché
la trasmutazione, il cambiamento d'identità degli elementi, divenne
possibile solo a partire dagli anni 1930-38 quando i fisici italiani (Fermi)
e tedeschi (Hahn) scoprirono il modo di produrre elementi artificiali tramite
reazioni nucleari e non chimiche. In questo corso vedremo la "trasmutazione"
di rame oppure mercurio in argento!

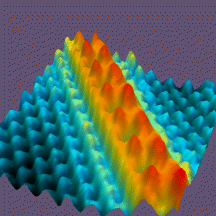
Alla base del progresso scientifico degli ultimi tre secoli ritroviamo il pensiero atomistico. Robert Boyle nel 1661 e Antoine Lavoisier nel 1789 definirono che cos'è veramente un elemento chimico. John Dalton enunciò nel 1808 la sua teoria atomistica e corpuscolare che spiegava in termini elementari le leggi della chimica (conservazione della massa, legge delle proporzioni di Proust). Ma gli atomi chi li ha mai visti?
 |
|
 |
|
|
|
 |
|
 |
|
 |
|
 |
|
In conclusione, l'antica idea di Democrito e Leucippo si dimosta esatta: la struttura e le trasformazioni della materia si lasciano spiegare sulla base di "mattoni" fondamentali e indivisibili di materia, gli atomi, di ben 107-109 tipi diversi, i quali possono legarsi tra di loro in modi diversi per formare i differenti stati di aggregazione della materia e tutte le sue sostanze. L'atomo è l'unità di materia di base degli elementi metallici, ma la molecola, una struttura superiore costruita da atomi, è la base per tutti i composti (sale, zucchero, anidride carbonica) ed alcuni elementi gassosi o non-metallici (zolfo, fosforo, ossigeno, azoto, carbonio, cloro).
|
|
|
PREVIOUS |
|
PHOTO GALLERY |
|
Last updated: Jan 2002!